化学、電池について学習しました。
気にしてみると、充電池ってけっこう医療現場使われているなぁと。
人工呼吸器、輸液ポンプ、心電図モニターなど、電源を入れたまま移動したい時に、コンセントを抜いてもバッテリーに切り替わるため使うことができるようになっています。
また、病院には病院全体の非常用電源があり、ここにもバッテリーが使われています。
病院には白、赤、緑と、色の違うコンセントがあるのですが、機器によって何色に差すかが決まっています。
その理由は、病院電気設備の安全基準というJIS規格があり、停電してから非常用電源が起動する時間が色により定められているからです。
赤は一般非常電源で、40秒以内に電気が供給され、
緑は無停電非常電源で、電気が途切れることなく供給されなければならない、
と決まっています。
白は普通の電気のため、医療機器系を差してはダメなのです。
調べてみると、病院の非常用電源のバッテリーとしては鉛蓄電池が多く使われているとのこと。
出典:https://www.baj.or.jp/battery/qa/gu58lf0000001e7a-img/12_01.gif
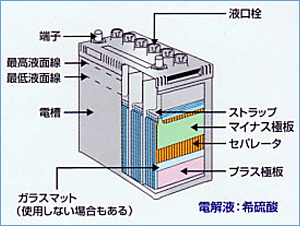
鉛蓄電池とは、
正極板に酸化鉛(PbO2)、負極板に鉛(Pb)、そして電解液に希硫酸(H2SO4)を使用しています。
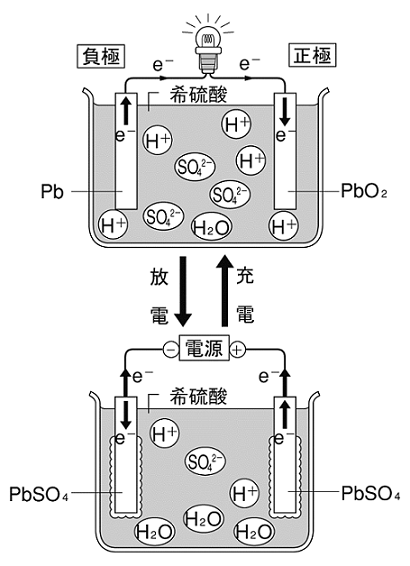
放電時、
負極の反応は、Pb + SO42-→ + PbSO4+2e– (酸化)
正極の反応は、PbO2+ SO42- + 4H+ + 2e– → PbSO4+ 2H2O (還元)
鉛と酸化鉛の酸化還元反応に、
希硫酸が電離して存在している硫酸イオン(SO42-)が反応し、硫酸鉛(PbSO4)が生成されます。
この酸化還元反応における電子の流れが電流となり、外部回路を通じて流れ、電力が供給されます。
充電時にはこれらの反応が逆に進行し、電池は再び充電され、電力を蓄えることができる仕組みになっています。
出典:https://jidoshaseibishi.com/chemistry/02/02.html
ここで疑問に思ったことは、
この酸化還元反応により生まれる電気は一定方向に流れる直流、
一方、コンセントから供給される電気は大きさや向きが変化する交流、
なのに機械が使えるの? ということ。
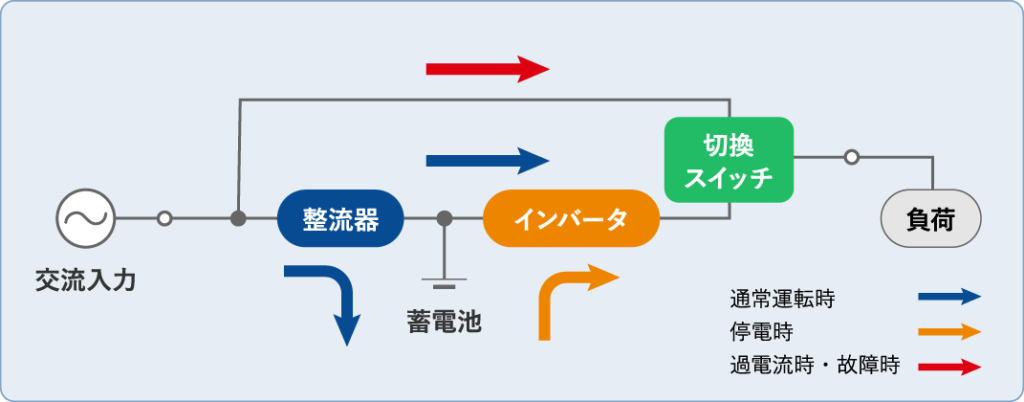
この秘密は、UPS(無停電電源装置)の中にある整流器とインバーターという機械にあるようです。
病院の非常用電源に使用されているUPSは、電力が途絶えた場合でも機器に電力を供給し続ける装置です。
出典: https://www.powers-inc.co.jp/products/ups
整流器は通常時に交流を直流に変換してバッテリーを充電し、インバーターは停電時にバッテリーの直流を交流に変換して機器に供給します。
この装置によって、バッテリーからの電力で医療機器が使えるようになっているんですね。
ちょっと外れてしまいましたが、電池を学習する中で病院の非常用の電源についても知ることができました。
<参照>



コメント